La producción de antibióticos está entrando en una etapa decisiva. La presión de la resistencia antimicrobiana y los avances en biotecnología están forzando a la industria a replantear cómo se diseñan y fabrican estos fármacos. Un análisis reciente publicado en Science Direct sitúa al sector en un punto de inflexión: mantener la eficacia terapéutica ya no depende solo de producir más, sino de producir mejor.
La resistencia antimicrobiana no es una amenaza lejana, es un problema creciente que ya condiciona decisiones industriales y sanitarias. ¿Cómo responder cuando los tratamientos clásicos empiezan a fallar? La respuesta pasa por combinar innovación científica con cambios en los modelos de producción.
La fermentación sigue siendo clave, pero ya no es la misma
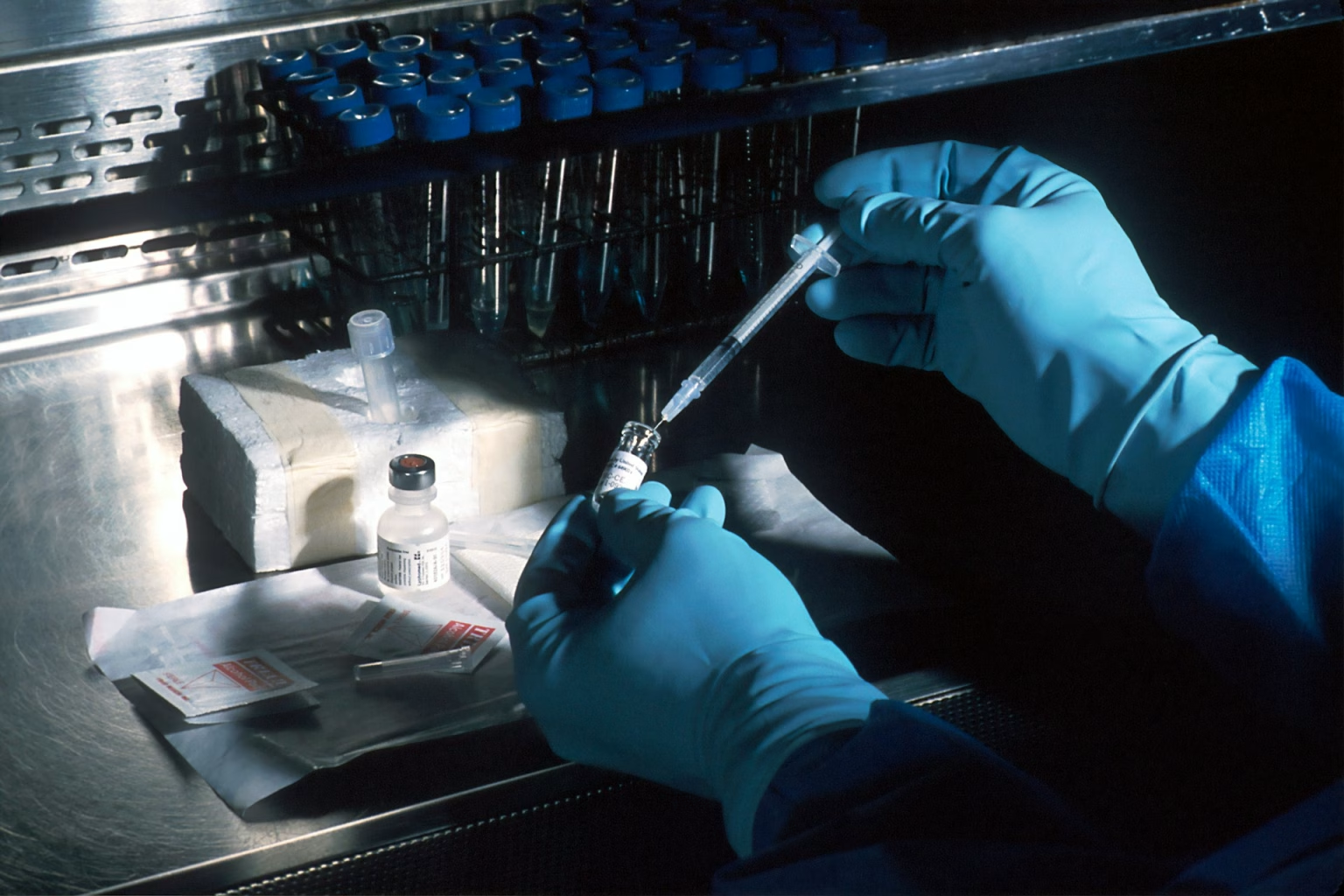
Uno de los pilares históricos, la fermentación microbiana, se mantiene. Sigue siendo el método más eficiente para producir antibióticos a gran escala, especialmente en medicamentos ampliamente utilizados como la penicilina. Sin embargo, el proceso ha evolucionado.
Hoy, esta técnica se apoya en herramientas avanzadas que permiten aumentar el rendimiento y controlar mejor la calidad del producto final. El mercado vinculado a estas tecnologías supera los 35.000 millones de dólares, una cifra que refleja su peso dentro de la industria farmacéutica global.
Nuevos materiales para combatir bacterias resistentes
En paralelo, gana terreno una línea de innovación menos tradicional. El desarrollo de materiales antibacterianos, como biopolímeros y sistemas híbridos con nanopartículas, está ampliando el abanico de soluciones disponibles.
A diferencia de los antibióticos clásicos, que suelen atacar un único objetivo, estos nuevos enfoques introducen mecanismos múltiples de acción. Por ejemplo, un recubrimiento con nanopartículas puede dañar la membrana bacteriana y, al mismo tiempo, interferir en su metabolismo. Este enfoque reduce la capacidad de las bacterias para adaptarse y desarrollar resistencia.
Ingeniería molecular: diseñar antibióticos a medida
Otra de las palancas clave es la ingeniería molecular. La posibilidad de modificar rutas metabólicas o diseñar compuestos específicos está cambiando el proceso de descubrimiento y producción de antibióticos.
Esto permite dos avances concretos:
- Ampliar el espectro de acción, llegando a bacterias antes difíciles de tratar
- Mejorar la eficiencia industrial, optimizando microorganismos productores
Esta evolución no surge de la nada. Se apoya en décadas de avances en ingeniería genética, que ahora empiezan a trasladarse de forma más directa a la producción farmacéutica.
Un mercado que crece… y un problema que también
El sector vive una contradicción evidente. El mercado global de antibióticos continúa expandiéndose, impulsado por la demanda sanitaria y el envejecimiento de la población. Pero ese crecimiento convive con un uso excesivo y, en muchos casos, poco controlado.
El resultado es claro: la aparición de bacterias resistentes se acelera. El análisis advierte que, sin medidas coordinadas, la resistencia antimicrobiana podría provocar millones de muertes anuales en las próximas décadas.
Cambio de estrategia: menos uso, más control
Este contexto está obligando a cambiar las reglas del juego. Cada vez más actores, desde farmacéuticas hasta organismos internacionales, apuestan por enfoques más sostenibles.
Entre las principales líneas de acción destacan:
- Reducir el uso innecesario de antibióticos en medicina y ganadería
- Desarrollar terapias alternativas que complementen o sustituyan a los antibióticos
- Implementar políticas públicas que controlen su distribución y prescripción
El foco ya no está solo en innovar, sino en proteger la eficacia de los tratamientos existentes.
Un desafío global con respuestas desiguales
El problema no afecta a todos por igual. Los países con mayores recursos lideran la innovación tecnológica, mientras que otras regiones concentran gran parte de la producción y el consumo.
Este desequilibrio complica la gestión global. Por ejemplo, una regulación estricta en Europa pierde impacto si en otros mercados el acceso y uso de antibióticos sigue sin control suficiente. La resistencia no entiende de fronteras.
Hacia un modelo más complejo y regulado
Las tendencias actuales apuntan a un cambio estructural. La producción de antibióticos será cada vez más sofisticada, interdisciplinar y dependiente de la regulación sanitaria.
Biotecnología avanzada, nuevos materiales y políticas públicas ya no son líneas paralelas. Forman parte de una misma estrategia para garantizar que los antibióticos sigan funcionando en el futuro. La industria ya lo ha asumido: no se trata solo de descubrir nuevos fármacos, sino de asegurar que sigan siendo útiles cuando realmente se necesiten.